코로나 백신 개발 위해 국내 8개 기업이 팔 걷고 나선다
화이자와 모더나 백신 가격이 인상됐다는 외신 보도가 나오면서 정부는 국산 백신 개발의 시급성을 거듭 강조했다.
 뉴스1
뉴스1
[뉴스1] 이영성 기자 = 국내 제약·바이오기업들의 코로나19 백신들이 하나, 둘 임상3상 궤도에 올라서면서 상용화에 속도를 내고 있다.
SK바이오사이언스는 지난 6월 임상시험 마지막 단계인 3상 시험계획서를 식품의약품안전처에 제출한 상태로 내년 상반기 출시를 목표로 두고 있다. 제넥신은 지난 달 인도네시아에서 임상2·3상 승인을 받았다.
2일 제약·바이오업계에 따르면, 식약처에 코로나19 백신 개발을 위해 임상을 신청한 기업은 최소 8곳으로 집계된다.
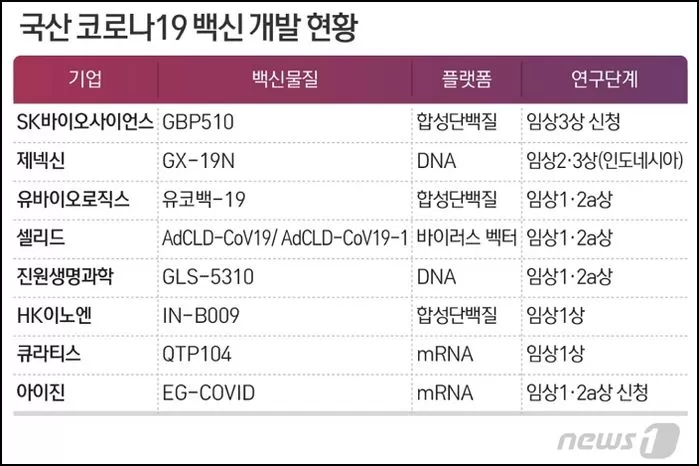
이들 기업은 △SK바이오사이언스 △제넥신 △HK이노엔(에이치케이이노엔) △유바이오로직스 △셀리드 △진원생명과학 △큐라티스 △아이진 등이다.
 뉴스1
뉴스1
SK바이오사이언스와 HK이노엔, 유바이오로직스의 백신 후보물질은 합성단백질 기술로 개발되고 있다는 점에서 미국 노바백스 백신과 플랫폼이 같다.
셀리드 백신은 아스트라제네카, 얀센 백신과 같은 바이러스 벡터 기반 기술로 개발되고 있다. 큐라티스와 아이진 백신은 화이자, 모더나 백신과 같은 mRNA 플랫폼 기술을 갖는다. 제넥신과 진원생명과학 백신의 경우 DNA 플랫폼 기술로 개발 중인데, 성공시 전세계 최초의 DNA 백신이 된다.
이 가운데 SK바이오사이언스와 제넥신이 개발 속도가 가장 빠르다. SK바이오사이언스는 자사의 코로나19 백신물질 'GBP510'에 대해 지난 6월 임상3상 신청을 한 뒤 식약처 승인을 기다리고 있다.
 뉴스1
뉴스1
GBP510은 빌&멜린다게이츠재단, CEPI(전염병대비혁신연합) 등의 지원을 받아 미국 워싱턴대학 항원디자인연구소(Institute for Protein Design, IPD)와 SK바이오사이언스가 공동 개발한 백신 후보물질이다.
임상 승인이 이뤄지면 SK바이오사이언스는 국제백신연구소(IVI)와 함께 유럽, 동남아 등 국가에서 임상3상 신청을 순차적으로 진행할 계획이다. 백신은 내년 상반기 상용화를 목표로 하고 있다.
특히 GBP510은 임상3상에서 유효성과 안전성을 입증할 경우 GBP510은 '코백스 퍼실리티’(COVAX facility)를 통해 수억회의 접종분이 전 세계에 공급돼 곧바로 글로벌시장 진출이 가능해진다.
 뉴스1
뉴스1
제넥신은 지난 7월 초 인도네시아 식약처(BPOM)으로부터 자사의 백신물질 'GX-19N'에 대한 임상2·3상 승인을 받았다.
제넥신은 인도네시아에서 5000명, 다른 국가에서 5000명을 모집해 총 1만명을 대상으로 임상3상을 진행할 계획이다. 이 과정에서 변이 바이러스에 대한 효과도 확인되면 임상 규모를 3만명으로 확대할 예정이다.
아울러 유바이오로직스가 현재 '유코백-19'에 대한 임상1·2a상(2상 전기)을 진행 중이고, 셀리드와 진원생명과학 역시 임상1·2a상을 하고 있다.
HK이노엔은 'IN-B009'에 대해 지난달 22일 임상1상 승인을 받았다. HK이노엔은 CJ제일제당 제약사업부가 전신으로, 현재 한국콜마그룹에 속해있다. 큐라티스도 자사의 백신물질 'QTP104'에 대해 지난달 19일 임상1상 승인을 받았다.
 뉴스1
뉴스1
국산 코로나19 치료제 개발에도 13개 기업이 뛰어든 상황이다. 올 2월 항체치료제(주사형) '렉키로나주'를 허가받고 출시한 셀트리온을 비롯해 △종근당 △대웅제약 △GC녹십자 △크리스탈지노믹스 △엔지켐생명과학 △신풍제약 △동화약품 △이뮨메드 △GC녹십자웰 △한국유나이티드제약 △뉴젠테라퓨틱스 △부광약품 등이다.
다만 GC녹십자가 개발한 코로나19 혈장분획치료제 '지코비딕주'는 지난 5월 식약처 검증 자문단 회의 결과 임상2상에서 효과 입증에 실패한 바 있다. 당시 GC녹십자는 추후 의료현장에서 활용 방안을 모색하겠다는 입장을 밝혔다.
그 외 대웅제약과 종근당, 신풍제약이 임상2상에서 효과 최종 목표치를 달성하지 못했지만, 각기 임상3상 혹은 다른 방식의 임상을 신청했거나 진행할 예정이다. 셀트리온은 미국 바이오기업 '인할론 바이오파마'와 함께 흡입형 렉키로나 개발에도 착수한 상황이다.
 기사의 이해를 돕기 위한 자료 사진 / gettyimagesBank
기사의 이해를 돕기 위한 자료 사진 / gettyimagesBank
한편 이날 화이자와 모더나 백신 가격이 인상됐다는 외신 보도가 나오면서, 정부는 국산 백신 개발의 시급성을 거듭 강조했다.
손영래 중앙사고수습본부 사회전략반장은 2일 출입기자단과 가진 백브리핑에서 "백신을 공급하는 회사는 소수에 불과하다 보니 공급자가 구매자보다 우위에 있다"면서 "중장기적으로 국내 백신을 확보하는 게 중요하다"고 밝혔다.
질병관리청은 올해 제2회 추가경정예산으로 3조6080억원을 확보해, 이중 1조5237억원을 국내외 개발 백신 구매비로 사용할 계획이다. 치료제 구입비로는 471억원이 책정됐다. 이중 중증 치료제 구매비는 248억원, 경·중등증 치료제 55억원, 경구용 치료제 168억원을 배정했다.